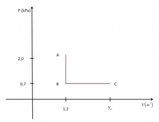
Un gas perfetto biatomico si trova alla temperatura di 35C e alla pressione di 6,00 atm. Dopo una trasformazione isocora, la sua pressione raggiunge il valore di 5,50 atm.
- Calcola la variazione di energia cinetica media delle molecole del gas.
Risoluzione
Sapendo che il gas subisce una trasformazione isocora, cio a volume costante, applichiamo la seconda legge di Gay-Lussac per trovare la temperatura finale del gas.
[math] p = frac(p_0)(T_0) T o p T_0 = p_0 T o T = p frac(T_0)(p_0) [/math]
Prima di applicare la formula trasformiamo i dati forniti dal problema nelle giuste unit di misura:
[math] T_0 = 35 C = 35 + 273,15 = 308,15 K[/math]
[math]p_0 = 6,00 atm = 6,00 \cdot 1,01 \cdot 10^5 Pa = 6,06 \cdot 10^5 Pa [/math]
[math]p = 5,50 atm = 5,50 \cdot 1,01 \cdot 10^5 Pa = 5,56 \cdot 10^5 Pa [/math]
Applichiamo la legge:
[math] T = pfrac(T_0)(p_0) =5,56 \cdot 10^5 Pa \cdot frac(308,15 K)(6,06 \cdot 10^5 Pa) = 282,73 K = 2,83 \cdot 10^2 K[/math]
Poich il problema chiede di determinare la variazione di energia cinetica del gas, cio lenergia cinetica finale meno quella iniziale, calcoliamo questi due valori mediante la formula:
[math]k_m = l/2 k_B T[/math]
dove l rappresenta i gradi di libert del gas, che in questo caso, essendo biatomico, ne avr 5;
[math]k_B[/math]
la costante di Boltzmann e vale [math] 1,38 \cdot 10^{-23} J/K[/math]
e T la temperatura del gas in kelvin.
[math]k_m (i) = 5/2 \cdot 1,38 \cdot 10^{-23} J/K \cdot 318,15 K = 1063,12 \cdot 10^{-23} J[/math]
[math]k_m (f) = 5/2 \cdot 1,38 \cdot 10^{-23} J/K \cdot 282,73 K = 975,42 \cdot 10^{-23} J[/math]
Calcoliamo ora la variazione di energia cinetica:
[math]?k =k_m (f) -k_m (i) =975,42 \cdot 10^{-23} J -1063,12 \cdot 10^{-23} J = [/math]
[math] -8,77 \cdot 10^{-23} J [/math]