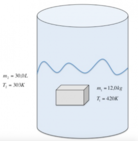
Un pezzo di metallo di massa
[math]100 g[/math]
ha una temperatura di [math]150 C[/math]
. Dopo essere stato immerso in [math]50 g[/math]
di acqua, che si trovava inizialmente alla temperatura di [math]20 C[/math]
, il metallo e lacqua raggiungono una temperatura di equilibrio di [math]40 C[/math]
.- Qual il calore specifico del metallo?
Svolgimento
Analizziamo i dati che abbiamo e trasformiamoli nelle giuste unit di misura:
[math] m_1 = 100 g = 100 \cdot 10^{-3} kg [/math]
[math] m_2 = 50 g = 50 \cdot 10^{-3} kg [/math]
[math]t_1 = 150C = 150 + 273,15 = 423,15 K [/math]
[math] t_2 = 20C = 20 + 273,15 = 293,15 K [/math]
Sappiamo inoltre che:
[math] c_a = 4186 frac(J)(kg \cdot K) , t_e = 40C = 40 + 273,15 = 313,15 K [/math]
Affinch vi sia equilibrio termico necessario che non vi siano scambi di energia fra le masse in
questione, cio che la somma dellenergia scambiata dallacqua e quella scambiata dallalluminio sia nulla, cio:
[math] Q_1 + Q_2 = 0 [/math]
Sappiamo che lenergia scambiata data dalla formula:
[math] Q = cm ?T [/math]
quindi:
[math] c_1 m_1 ?T_1 + c_2 m_2 ?T_2 = 0 [/math]
[math] ?T[/math]
la variazione di temperatura, cio la temperatura finale meno quella iniziale.
[math] ?T = T_f - T_i [/math]
Abbiamo la temperatura iniziale di entrambi i materiali, e anche quella finale, rappresentata dalla temperatura di equilibrio.
[math] c_1 m_1 (T_e - T_(i_1))_1 + c_2 m_2 (T_e - T_(i_2))_2 = 0 [/math]
Ricaviamo dalla formula il calore specifico del metallo:
[math] c_1 m_1 (T_e - T_(i_1))_1 = - c_2 m_2 (T_e - T_(i_2))_2 [/math]
[math] c_1 = - frac(c_2 m_2 (T_e - T_(i_2))_2)(m_1 (T_e - T_(i_1))_1) [/math]
Sostituiamo i dati e ricaviamo il valore del calore specifico:
[math] c_1 = - frac(4186 \cdot 50 \cdot 10^{-3} \cdot (313,15 - 293,15))( 100 \cdot 10^{-3} (313,15 - 423,15)) = [/math]
[math] - frac(4186 \cdot 50 \cdot 10^{-3} \cdot 20)( 100 \cdot 10^{-3} (- 100)) = 380,5 frac(J)(kg \cdot K) = 3,0 \cdot 10^2 frac(J)(kg \cdot K) [/math]