Abbiamo già visto in precedenza che esistono alcuni tipi di trasformazioni che avvengono mantenendo costante uno dei parametri fondamentali, come nel caso delle trasformazioni isobare, isocore e isoterme.
Vediamo, ora, altre due importanti categorie di trasformazioni, che sono le perforazioni reversibili e irreversibili.
Trasformazioni reversibili
Come sappiamo, una trasformazione termodinamica fa si che, partendo da uno stato iniziale i, il sistema arriverà ad uno stato finale f, avendo modificato, nel corso della trasformazione, alcuni delle sue proprietà.
Supponiamo di voler riportare il sistema dallo stato finale a quello iniziale, cioè di voler compiere una trasformazione inversa.
Trasformazioni irreversibili
Supponiamo che sia possibile riportare il sistema allo stato originale; lo stato, quindi, può tornare a quello che era prima della trasformazione. La trasformazione che il sistema ha subito viene definita reversibile. In questi casi, sia il sistema che l’ambiente ritornano allo stato originale mediante una trasformazione inversa.
Se non è possibile, invece, riportare il sistema nello stato originale senza modificare l’ambiente circostante, si dice che la trasformazione è irreversibile.
In generale, in natura, quasi tutti i fenomeni spontanei sono irreversibili; infatti, in genere, non è possibile far ritornare sia il sistema che l’ambiente alle condizioni che avevano nello stato iniziale.
Tuttavia, in termodinamica è spesso conveniente lavorare con fenomeni reversibili; grazie ad essi, infatti, è possibile studiare determinate caratteristiche delle trasformazioni.
In generale, affinché una trasformazione sia reversibile è necessario che siano soddisfatte determinate condizioni:
- la trasformazione deve essere quasistatica;
In una trasformazione quasistatica, infatti, in ogni istante la pressione e la temperatura del sistema differiscono di una quantità infinitesima rispetto allo stato precedente.
Gli stati che rappresentano la trasformazione sono praticamente infiniti; tuttavia si può ipotizzare di considerare due stati intermedi della trasformazione, nei quali è avvenuta uno scambio infinitesimo di calore ∆Q.
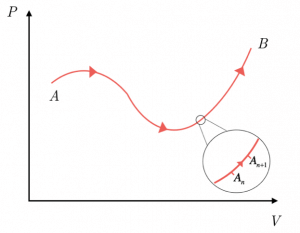
E’ possibile riportare il sistema allo stato precedente fornendo al sistema uno scambio di calore opposto, cioè -∆Q.
Operando in questo modo per tutti gli stati intermedi infinitesimi della trasformazione è teoricamente possibile far ritornare il sistema alla situazione originaria.
- Il sistema scambi deve scambiare calore solamente con sorgenti ideali di calore.
In questo caso, infatti, è possibile che nella trasformazione vi sono sorgenti che cedono calore, e altre che lo ricevono; questo processo è responsabile di una modifica dell’ambiente. Nel processo inverso è possibile ritornare alla situazione originaria semplicemente con uno scambio inverso di calore; si opera in modo che le sorgenti che prima ne avevano ceduto, ora ne acquistino una quantità uguale, e viceversa.
Il caso delle combustioni
Le combustioni non rappresentano trasformazioni reversibili. Quando si sfrutta una combustione per aumentare la temperatura di un determinato sistema, ad esempio, sembrerebbe possibile far tornare il sistema alla situazione iniziale semplicemente mettendolo in un ambiente più freddo del precedente. Questo, in effetti, permetterebbe al sistema di riacquistare la sua temperatura iniziale.
Tuttavia, affinché la trasformazione sia reversibile, è necessario che anche l’ambiente torni nella sua condizione iniziale. Come sappiamo, le combustioni avvengono con consumo di ossigeno e carbonio e produzione di anidride carbonica.
Di conseguenza, in seguito alla reazione, la composizione di questi elementi nell’ambiente è variata rispetto alla situazione iniziale, e non è possibile in alcun modo ripristinarla attraverso un processo inverso.
- Durante la trasformazione deve essere assente qualsiasi forza dissipativa.
Possiamo immaginare, quindi, che la maggior parte (se non tutte) delle trasformazioni che avvengono in natura sono irreversibili; infatti è impossibile eliminare del tutto le forze dissipative che agiscono nel corso della trasformazione, come ad esempio le forze di attrito.
Nel caso in cui agisse una forza di attrito, infatti, non sarebbe sufficiente invertire semplicemente i processi di trasformazione, fornendo quantità opposte di scambi di calore. Vi è, infatti, un lavoro che viene svolto anche dalla forza di attrito nel corso della trasformazione, che da luogo ad una quantità di energia che viene dissipata; di conseguenza, la quantità di calore da fornire nel processo inverso dovrebbe essere maggiore di quella che è stata scambiata nel processo iniziale.
Potrebbero interessarti
Appunti: Il teorema di Carnot
Appunti: La disuguaglianza di Clausius e l’entropia
Appunti: L’entropia nei sistemi isolati e non isolati
